Автор:
Randy Alexander
Дата На Създаване:
2 Април 2021
Дата На Актуализиране:
1 Юли 2024
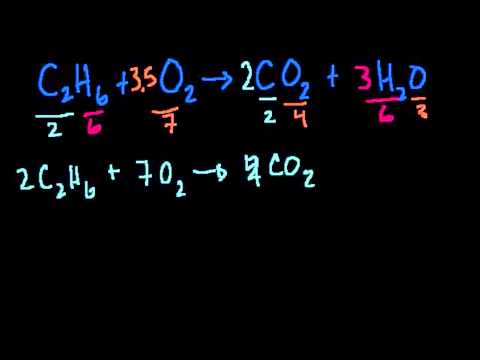
Съдържание
Химическото уравнение е символично представяне на химична реакция. Реактивите са написани от лявата страна, а продуктът от дясната страна. Законът за запазване на масата показва, че нито един атом не се ражда или губи при химична реакция, така че броят на атомите, присъстващи в реагента, трябва да бъде равен на броя на атомите, присъстващи в реакцията. продукт. Следвайки този урок, можете да балансирате химическите уравнения по различни начини.
Стъпки
Метод 1 от 2: Баланс съгласно традиционния метод
Напишете даденото уравнение. В този пример ще имате: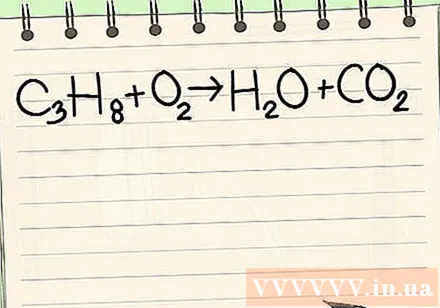
- ° С3З.8 + O2 -> H2O + CO2
- Тази реакция възниква, когато пропан (C3З.8изгаря в кислород, за да образува вода и въглероден диоксид.

Запишете броя на атомите за всеки елемент, който имате от всяка страна на уравнението. Вижте индексите по-долу до всеки атом, за да намерите броя на атомите в уравнението.- Вляво: 3 въглерода, 8 водорода и 2 кислорода.
- Вдясно: 1 въглерод, 2 водорода и 3 кислорода.
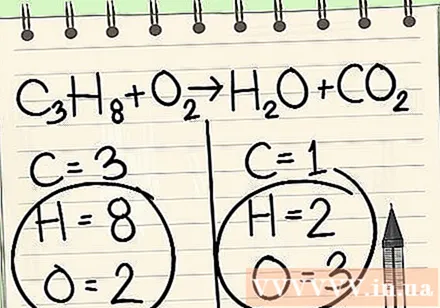
Винаги оставяйте водород и кислород накрая.
Ако ви остават повече от един елемент за балансиране: Изберете елемент, който се появява само в единичната молекула на реагента и само в единичната молекула на продукта. Това означава, че първо ще трябва да балансирате въглеродните атоми.
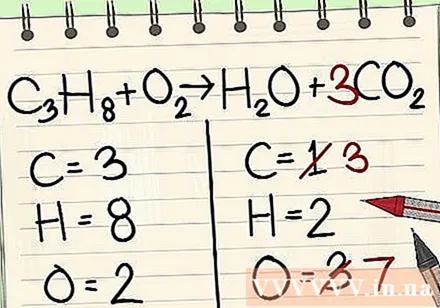
Добавете коефициента за единични въглеродни атоми от дясната страна на уравнението, за да го балансирате с трите въглеродни атома от лявата страна на уравнението.- ° С3З.8 + O2 -> H2O + 3CO2
- Фактор 3 пред въглерода от дясната страна показва, че има 3 въглеродни атома, точно както индексът под 3 от лявата страна показва 3 въглеродни атома.
- В химическо уравнение можете да промените коефициента, но не и индекса.
Следва атомният баланс на водорода. Имате 8 водородни атома вляво. Следователно ще ви трябват 8 от дясната страна.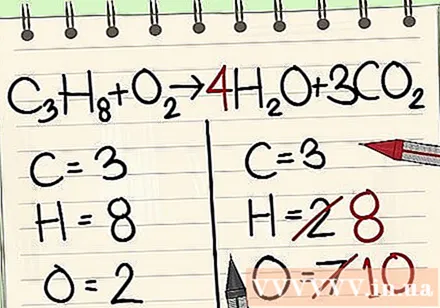
- ° С3З.8 + O2 -> 4Н2O + 3CO2
- Вдясно от часа добавяте 4 като фактор, защото долното число показва, че вече имате 2 водородни атома.
- Когато умножите фактор 4 по индекс 2, получавате 8.
- Останалите 6 кислородни атома са от 3CO2. (3x2 = 6 кислородни атома + 4 други кислородни атома = 10)
Балансират кислородните атоми.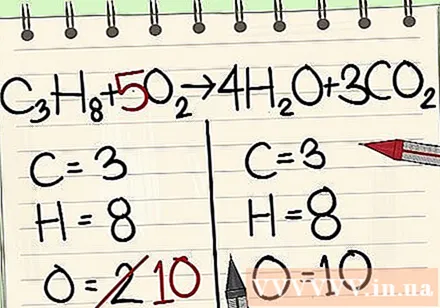
- Тъй като сте добавили коефициенти към молекулите вдясно от уравнението, броят на кислородните атоми се е променил. Сега имате 4 кислородни атома във молекулата на водата и 6 кислородни атома в молекулата на въглеродния диоксид. Общо имаме 10 кислородни атома.
- Добавете фактор 5 към молекулата на кислорода вляво от уравнението. Сега имате 10 молекули кислород от всяка страна.
- ° С3З.8 + 5O2 -> 4Н2O + 3CO2.

- Въглеродните, водородните и кислородните атоми са в баланс. Вашето уравнение е завършено.
Метод 2 от 2: Баланс според алгебричния метод
Напишете уравнения според символи и формули. Пример a = 1 и напишете уравнението въз основа на тази формула.
Заменете цифрите с техните променливи.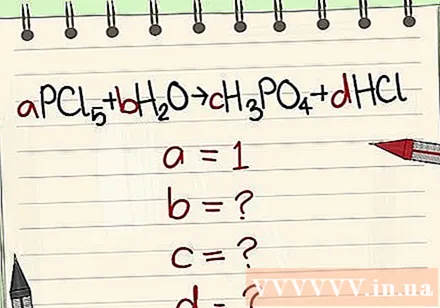
Проверете количеството елементи в реакционната страна, както и в продукта.
- Пример: aPCl5 + bH2O = cH3PO4 + dHCl, така че a = 1 b = c = d = и разделяне на елементите P, Cl, H, O, така че получавате a = 1 b = 4 c = 1 d = 5 .
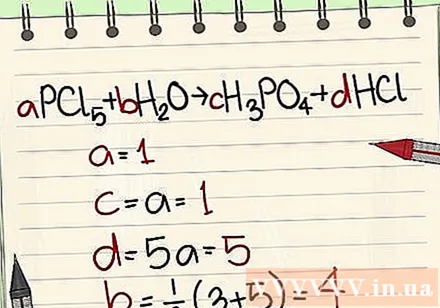
- Пример: aPCl5 + bH2O = cH3PO4 + dHCl, така че a = 1 b = c = d = и разделяне на елементите P, Cl, H, O, така че получавате a = 1 b = 4 c = 1 d = 5 .
Съвети
- Не забравяйте да опростите уравнението.
- Ако имате проблеми, можете да въведете уравнение в инструмента за онлайн баланс, за да го балансирате. Не забравяйте, че когато полагате изпита, нямате достъп до онлайн баланс, така че не зависи от него.
Внимание
- Никога не използвайте коефициент като част от химическото уравнение - не можете да разделяте молекули или атоми при химична реакция.
- По време на процеса на уравновесяване можете да използвате дроби, но уравнението няма да бъде балансирано, ако коефициентите все още са дроби.
- За да премахнете фракциите, умножете цялото уравнение (отляво и отдясно) по знаменателя на фракцията.



