Автор:
Clyde Lopez
Дата На Създаване:
26 Юли 2021
Дата На Актуализиране:
1 Юли 2024

Съдържание
- Стъпки
- Метод 1 от 4: Изчисляване на процента с помощта на формула за тегло / обем
- Метод 2 от 4: Приготвяне на молекулен разтвор
- Метод 3 от 4: Разреждащи разтвори с известна концентрация
- Метод 4 от 4: Спазване на мерките за безопасност
- Съвети
- Предупреждения
- Какво ти е необходимо
Простите химически разтвори могат лесно да се приготвят по различни начини у дома или на работното място. Независимо дали правите разтвор от прахообразен материал или разреждате течност, лесно е да определите правилното количество на всеки компонент. Когато приготвяте химически разтвори, не забравяйте да използвате лични предпазни средства, за да избегнете повреди.
Стъпки
Метод 1 от 4: Изчисляване на процента с помощта на формула за тегло / обем
 1 Определете процент съдържание на тегло/ обем разтвор. Процентите показват колко части от веществото са в сто части от разтвора. Когато се прилага към химически разтвори, това означава, че ако концентрацията е 1 процент, тогава 100 милилитра разтвор съдържа 1 грам от веществото, тоест 1 ml / 100 ml.
1 Определете процент съдържание на тегло/ обем разтвор. Процентите показват колко части от веществото са в сто части от разтвора. Когато се прилага към химически разтвори, това означава, че ако концентрацията е 1 процент, тогава 100 милилитра разтвор съдържа 1 грам от веществото, тоест 1 ml / 100 ml. - Например, тегловно: 10% тегловен разтвор съдържа 10 грама вещество, разтворено в 100 милилитра разтвор.
- Например, по обем: 23 процентен обем разтвор съдържа 23 милилитра течно съединение на всеки 100 милилитра разтвор.
 2 Определете обема на разтвора, който искате да приготвите. За да разберете необходимата маса на дадено вещество, първо трябва да определите крайния обем на разтвора, от който се нуждаете. Този обем зависи от това колко разтвор се нуждаете, колко често ще го използвате и стабилността на готовия разтвор.
2 Определете обема на разтвора, който искате да приготвите. За да разберете необходимата маса на дадено вещество, първо трябва да определите крайния обем на разтвора, от който се нуждаете. Този обем зависи от това колко разтвор се нуждаете, колко често ще го използвате и стабилността на готовия разтвор. - Ако трябва да използвате пресен разтвор всеки път, пригответе само необходимото количество за една употреба.
- Ако разтворът запазва свойствата си за дълго време, можете да приготвите по -голямо количество, за да го използвате по -късно.
- Пример: Трябва да приготвите 5% разтвор на NaCl с обем 500 ml.
 3 Изчислете броя грамове на веществото, необходимо за приготвяне на разтвора. За да изчислите необходимия брой грамове, използвайте следната формула: брой грамове = (необходим процент) (необходим обем / 100 ml). В този случай необходимите проценти се изразяват в грамове, а необходимия обем в милилитри.
3 Изчислете броя грамове на веществото, необходимо за приготвяне на разтвора. За да изчислите необходимия брой грамове, използвайте следната формула: брой грамове = (необходим процент) (необходим обем / 100 ml). В този случай необходимите проценти се изразяват в грамове, а необходимия обем в милилитри. - Пример: Трябва да приготвите 5% разтвор на NaCl с обем 500 ml.
- брой грамове = (5g) (500ml / 100ml) = 25 грама.
- Ако NaCl се дава като разтвор, просто вземете 25 милилитра NaCl вместо грамове прах и извадете този обем от крайния обем: 25 милилитра NaCl до 475 милилитра вода.
 4 Претеглете веществото. След като изчислите необходимата маса на веществото, трябва да измерите това количество. Вземете калибрирана скала, поставете купа върху нея и задайте нула. Претеглете необходимото количество вещество в грамове и го излейте.
4 Претеглете веществото. След като изчислите необходимата маса на веществото, трябва да измерите това количество. Вземете калибрирана скала, поставете купа върху нея и задайте нула. Претеглете необходимото количество вещество в грамове и го излейте. - Преди да продължите да приготвяте разтвора, не забравяйте да почистите тенджерата за прах от остатъците от прах.
- В горния пример трябва да претеглите 25 грама NaCl.
 5 Разтворете веществото в необходимото количество течност. Освен ако не е посочено друго, като разтворител се използва вода. Вземете мерителна чаша и измерете необходимото количество течност. След това прахът се разтваря в течността.
5 Разтворете веществото в необходимото количество течност. Освен ако не е посочено друго, като разтворител се използва вода. Вземете мерителна чаша и измерете необходимото количество течност. След това прахът се разтваря в течността. - Подпишете контейнера, в който ще съхранявате разтвора. Ясно посочете веществото и неговата концентрация върху него.
- Пример: Разтворете 25 грама NaCl в 500 милилитра вода, за да направите 5% разтвор.
- Не забравяйте, че ако разреждате течно вещество, за да получите необходимото количество вода, извадете обема на добавеното вещество от крайния обем на разтвора: 500 ml - 25 ml = 475 ml вода.
Метод 2 от 4: Приготвяне на молекулен разтвор
 1 Определете молекулното тегло на използваното вещество, като използвате формулата. Теглото на формулата (или просто молекулното тегло) на съединението е написано в грамове на мол (g / mol) върху стената на бутилката. Ако не можете да намерите молекулното тегло на бутилката, потърсете онлайн.
1 Определете молекулното тегло на използваното вещество, като използвате формулата. Теглото на формулата (или просто молекулното тегло) на съединението е написано в грамове на мол (g / mol) върху стената на бутилката. Ако не можете да намерите молекулното тегло на бутилката, потърсете онлайн. - Молекулното тегло на веществото е масата (в грамове) на един мол от това вещество.
- Пример: Молекулното тегло на натриев хлорид (NaCl) е 58.44 g / mol.
 2 Определете обема на необходимия разтвор в литри. Приготвянето на един литър разтвор е много лесно, тъй като моларността му се изразява в молове / литър, но може да се наложи да се направят повече или по -малко литри в зависимост от целта на разтвора. Използвайте крайния обем, за да изчислите необходимия брой грамове.
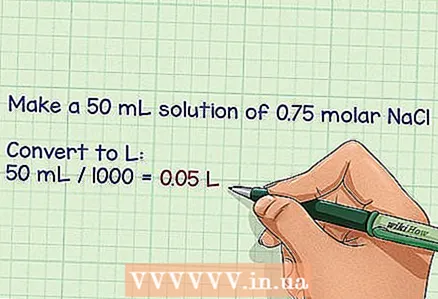
2 Определете обема на необходимия разтвор в литри. Приготвянето на един литър разтвор е много лесно, тъй като моларността му се изразява в молове / литър, но може да се наложи да се направят повече или по -малко литри в зависимост от целта на разтвора. Използвайте крайния обем, за да изчислите необходимия брой грамове. - Пример: необходимо е да се приготвят 50 ml разтвор с моларна фракция на NaCl от 0,75.
- За да преобразувате милилитри в литри, разделете ги на 1000 и получете 0,05 литра.
 3 Изчислете броя на грамовете, необходими за приготвяне на необходимия молекулен разтвор. За да направите това, използвайте следната формула: брой грамове = (необходим обем) (необходима моларност) (молекулно тегло съгласно формулата). Не забравяйте, че необходимия обем се изразява в литри, моларността е в молове на литър, а молекулното тегло по формулата е в грамове на мол.
3 Изчислете броя на грамовете, необходими за приготвяне на необходимия молекулен разтвор. За да направите това, използвайте следната формула: брой грамове = (необходим обем) (необходима моларност) (молекулно тегло съгласно формулата). Не забравяйте, че необходимия обем се изразява в литри, моларността е в молове на литър, а молекулното тегло по формулата е в грамове на мол. - Пример: ако искате да приготвите 50 милилитра разтвор с моларна част от NaCl 0,75 (молекулно тегло по формулата: 58,44 g / mol), трябва да изчислите броя на грамовете NaCl.
- брой грамове = 0,05 l * 0,75 mol / l * 58,44 g / mol = 2,19 грама NaCl.
- Чрез намаляване на мерните единици получавате грам вещество.
 4 Претеглете веществото. Претеглете необходимото количество, като използвате правилно калибрирана везна. Поставете купа на везната и нула преди претегляне. Добавете веществото в купата, докато достигнете желаната маса.
4 Претеглете веществото. Претеглете необходимото количество, като използвате правилно калибрирана везна. Поставете купа на везната и нула преди претегляне. Добавете веществото в купата, докато достигнете желаната маса. - Почистете теглилката след употреба.
- Пример: Претеглете 2,19 грама NaCl.
 5 Разтворете праха в необходимото количество течност. Освен ако не е посочено друго, повечето разтвори използват вода. В този случай се взема същия обем течност, който е използван за изчисляване на масата на веществото. Добавете вещество към водата и разбъркайте, докато се разтвори напълно.
5 Разтворете праха в необходимото количество течност. Освен ако не е посочено друго, повечето разтвори използват вода. В този случай се взема същия обем течност, който е използван за изчисляване на масата на веществото. Добавете вещество към водата и разбъркайте, докато се разтвори напълно. - Подпишете контейнера с разтвора. Ясно маркирайте разтвореното вещество и моларността, за да можете да използвате разтвора по -късно.
- Пример: С помощта на чаша (инструмент за измерване на обема) отмервайте 50 ml вода и разтворете 2,19 грама NaCl в нея.
- Разбъркайте разтвора, докато прахът се разтвори напълно.
Метод 3 от 4: Разреждащи разтвори с известна концентрация
 1 Определете концентрацията на всеки разтвор. Когато разреждате разтвори, трябва да знаете концентрацията на първоначалния разтвор и разтвора, който искате да получите.Този метод е подходящ за разреждане на концентрирани разтвори.
1 Определете концентрацията на всеки разтвор. Когато разреждате разтвори, трябва да знаете концентрацията на първоначалния разтвор и разтвора, който искате да получите.Този метод е подходящ за разреждане на концентрирани разтвори. - Пример: Пригответе 75 милилитра 1,5 М разтвор на NaCl от 5 М разтвор. Основният разтвор има концентрация 5 М и е необходимо да се разрежда до концентрация 1,5 М.
 2 Определете обема на крайния разтвор. Необходимо е да намерите обема на решението, което искате да получите. Ще трябва да изчислите количеството разтвор, което ще бъде необходимо за разреждане на този разтвор до желаната концентрация и обем.
2 Определете обема на крайния разтвор. Необходимо е да намерите обема на решението, което искате да получите. Ще трябва да изчислите количеството разтвор, което ще бъде необходимо за разреждане на този разтвор до желаната концентрация и обем. - Пример: Пригответе 75 милилитра от 1,5 М разтвор на NaCl от първоначален разтвор от 5 М. В този пример крайният обем на разтвора е 75 милилитра.
 3 Изчислете обема на разтвора, необходим за разреждане на изходния разтвор. За да направите това, имате нужда от следната формула: V1° С1= V2° С2където V1 - обемът на необходимия разтвор, C1 - неговата концентрация, V2 - обем на крайния разтвор, C2 - концентрацията му.
3 Изчислете обема на разтвора, необходим за разреждане на изходния разтвор. За да направите това, имате нужда от следната формула: V1° С1= V2° С2където V1 - обемът на необходимия разтвор, C1 - неговата концентрация, V2 - обем на крайния разтвор, C2 - концентрацията му. - За да се изчисли обемът на необходимата течност, е необходимо да се пренапише равенството по отношение на V1: V1 = (V2° С2) / ° С1.
- Пример: Трябва да приготвите 75 ml разтвор на NaCl с концентрация 1,5 M от разтвор с концентрация 5 M.
- V1 = (V2° С2) / ° С1 = (0,075 л * 1,5 М) / 5 М = 0,0225 л.
- Конвертирайте литри обратно в милилитри, като умножите по 1000, за да получите 22,5 милилитра.
 4 Извадете обема на оригиналния разтвор от планирания краен обем. В резултат на разреждането на разтвора е необходимо да се получи фиксиран краен обем. Извадете обема на основния разтвор от крайния обем, за да определите обема на разтвора за разреждане.
4 Извадете обема на оригиналния разтвор от планирания краен обем. В резултат на разреждането на разтвора е необходимо да се получи фиксиран краен обем. Извадете обема на основния разтвор от крайния обем, за да определите обема на разтвора за разреждане. - Пример: Крайният обем е 75 милилитра, а първоначалният обем е 22,5 милилитра. Така получаваме 75 - 22,5 = 52,5 милилитра. Именно този обем течност ще бъде необходим за разреждане на разтвора.
 5 Смесете изчисленото количество основен разтвор с течността за разреждане. С помощта на чаша (инструмент за измерване на обема на течността), измерете необходимото количество от основния разтвор и го смесете с необходимия обем на разреждащата течност.
5 Смесете изчисленото количество основен разтвор с течността за разреждане. С помощта на чаша (инструмент за измерване на обема на течността), измерете необходимото количество от основния разтвор и го смесете с необходимия обем на разреждащата течност. - Пример: Измерете 22,5 милилитра 5 M разтвор на NaCl и разредете с 52,5 милилитра вода. Разбъркайте разтвора.
- Напишете върху контейнера с разредения разтвор неговата концентрация и състав: 1,5 M NaCl.
- Не забравяйте, че ако разреждате киселина с вода, трябва да добавите киселина във водата, но никога обратното.
Метод 4 от 4: Спазване на мерките за безопасност
 1 Използвайте лични предпазни средства. Когато работите с агресивни химикали и разтвори, предпазвайте се от тяхното въздействие. Не забравяйте да носите лабораторно палто, затворени обувки, предпазни очила и ръкавици.
1 Използвайте лични предпазни средства. Когато работите с агресивни химикали и разтвори, предпазвайте се от тяхното въздействие. Не забравяйте да носите лабораторно палто, затворени обувки, предпазни очила и ръкавици. - Използвайте лабораторно палто от негорим материал.
- Предпазните очила трябва да имат странични щитове, които покриват очите отстрани.
 2 Работете в добре проветриво помещение. При разбъркване на разтворите могат да се отделят летливи газове. Някои вещества трябва да се боравят само под лабораторен капак. Ако смесвате разтвори у дома, отворете прозорците и включете вентилатор, за да осигурите адекватна циркулация на въздуха.
2 Работете в добре проветриво помещение. При разбъркване на разтворите могат да се отделят летливи газове. Някои вещества трябва да се боравят само под лабораторен капак. Ако смесвате разтвори у дома, отворете прозорците и включете вентилатор, за да осигурите адекватна циркулация на въздуха.  3 Добавете киселина към водата. Когато разреждате концентрирани киселини, винаги добавяйте киселината към водата. При смесване на вода и киселина възниква екзотермична (с отделяне на топлина) реакция, която може да доведе до експлозия, ако към киселината се добави вода, а не обратното.
3 Добавете киселина към водата. Когато разреждате концентрирани киселини, винаги добавяйте киселината към водата. При смесване на вода и киселина възниква екзотермична (с отделяне на топлина) реакция, която може да доведе до експлозия, ако към киселината се добави вода, а не обратното. - Не забравяйте мерките за безопасност всеки път, когато работите с киселини.
Съвети
- Преди да започнете, запознайте се с темата. Знанието е сила!
- Опитайте да използвате обикновени домакински продукти. Не се опитвайте да направите нещо необикновено. Ако подозирате, че може да възникне опасност, откажете се.
Предупреждения
- Не смесвайте белина и амоняк.
- Използвайте предпазни средства, очила, пластмасова престилка и неопренови ръкавици, ако е необходимо.
Какво ти е необходимо
- Прецизни механични или електронни везни за определяне на масата. Например, можете да използвате кухненска везна.
- Градуирани стъклени изделия. Тези прибори могат да бъдат намерени в магазин за кухненски съдове или поръчани онлайн. Измервателното стъкло се предлага в различни форми и размери. Пластмасовите съдове ще работят, въпреки че няма да издържат на високи температури.



