Автор:
John Stephens
Дата На Създаване:
1 Януари 2021
Дата На Актуализиране:
29 Юни 2024

Съдържание
Били ли сте някога да оставяте бутилка вода на слънце за няколко часа, след това да отваряте капака и да чувате малко „пукане“? Този звук се дължи налягане на парите в бутилката с причината. В химията налягането на парите е налягането, действащо върху стената на затворен съд, тъй като течността в съда се изпарява (превръща се в газ). За да намерите налягането на парите при известна температура, използвайте уравнението на Клаузиус-Клапейрон: ln (P1 / P2) = (ΔHvap/ R) ((1 / T2) - (1 / T1)).
Стъпки
Метод 1 от 3: Използвайте уравнението на Клаузий-Клапейрон
Напишете уравнението на Клаузий-Клапейрон. Когато се разглежда промяната на налягането на парите във времето, формулата за изчисляване на налягането на парите е уравнението на Клаузий-Клапейрон (кръстено на физиците Рудолф Клаузиус и Беноа Пол Емил Клапейрон). Това е често използвана формула за решаване на често срещани проблеми с налягането на парите във физиката и химията. Формулата е написана по следния начин: ln (P1 / P2) = (ΔHvap/ R) ((1 / T2) - (1 / T1)). В тази формула променливите представляват: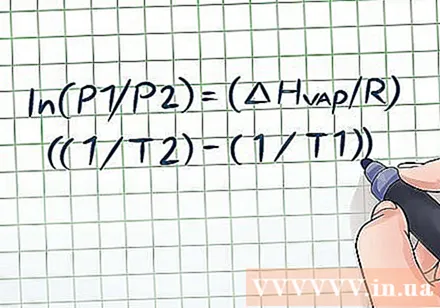
- ΔHvap: Енталпия на изпаряване на течности. Тази стойност може да бъде намерена в таблицата в края на учебник по химия.
- R: Идеална газова константа и равна на 8 314 J / (K × Mol).
- Т1: Температура, при която е известно налягането на парата (начална температура).
- Т2: Температурата, при която се изисква налягането на парите (крайна температура).
- P1 и P2: Съответното налягане на парите при температури T1 и T2.
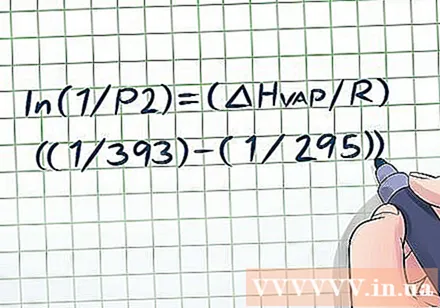
Заменете известните стойности на променливите. Уравнението на Клаузий-Клапейрон изглежда доста сложно, тъй като има много различни променливи, но не е твърде трудно, ако проблемът предоставя достатъчно информация. Най-основните проблеми с налягането на парата ще ви дадат две стойности на температурата и една стойност на налягането или две стойности на налягане и една стойност на температурата - след като имате тези данни, това е лесно за решаване.- Да предположим например, че проблемът е за съд с течност при 295 К и с парно налягане от 1 атмосфера (атм). Въпросът е: Какво е налягането на парата при температура 393 К? Имаме две стойности за температура и една за налягане, така че е възможно да се реши за останалото налягане, като се използва уравнението на Клаузиус-Клапейрон. Поставяме стойности в променливи, имаме ln (1 / P2) = (ΔHvap/ R) ((1/393) - (1/295)).
- За уравнението на Клаузиус-Клапейрон винаги трябва да използваме температурна стойност Келвин. Можете да използвате всяка стойност на налягането, стига тя да е в еднакви единици както за P1, така и за P2.
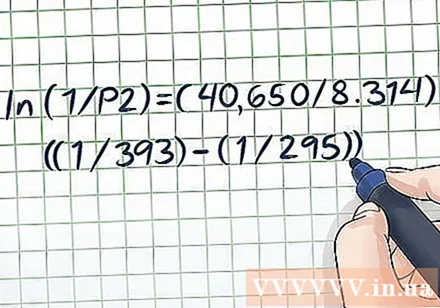
Заменете константите. Уравнението на Клаузий-Клапейрон има две константи: R и ΔHvap. R винаги е равен на 8 314 J / (K × Mol). Въпреки това, ΔHvap (летлива енталпия) зависи от вида на изпаряващата се течност, дадена от проблема. С това казано можете да търсите ΔH стойностиvap на различни вещества в края на учебника по химия или физика или го потърсете онлайн (напр. тук.)- В горния пример приемете, че течността е чиста вода. Ако погледнете в таблицата стойност Hvap, имаме ΔHvap пречистена вода е приблизително 40,65 kJ / mol. Тъй като стойността H използва джаулови единици, трябва да я преобразуваме в 40,650 J / mol.
- Поставяйки константи в уравнението, имаме ln (1 / P2) = (40,650 / 8,314) ((1/393) - (1/295)).
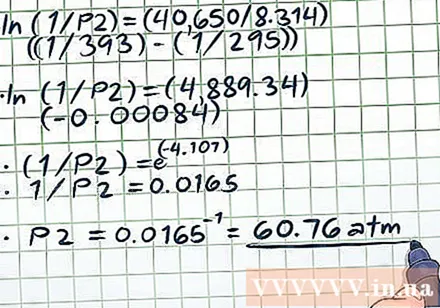
Решете уравнението. След като сте вмъкнали всички стойности в променливите на уравнението, с изключение на променливата, която изчисляваме, продължете да решавате уравнението според обичайния алгебричен принцип.- Най-трудната точка при решаване на уравнението (ln (1 / P2) = (40,650 / 8,314) ((1/393) - (1/295))) е обработката на естествената логаритмична функция (ln). За да елиминирате естествената функция на логаритъма, използвайте двете страни на уравнението като показател за математическата константа д. С други думи, ln (x) = 2 → e = e → x = e.
- Сега нека решим уравнението на примера:
- ln (1 / P2) = (40,650 / 8,314) ((1/393) - (1/295))
- ln (1 / P2) = (4,889.34) (- 0,00084)
- (1 / P2) = д
- 1 / P2 = 0,0165
- P2 = 0,0165 = 60,76 атм. Тази стойност е разумна - в затворен съд, когато температурата се повиши с почти 100 градуса (до температура приблизително 20 градуса над точката на кипене на водата), се образува много пара, така че налягането ще се увеличи. много.
Метод 2 от 3: Намерете налягането на парите на разтворения разтвор
Напишете закона на Раул. Всъщност рядко работим с чисти течности - често се налага да работим със смеси от много различни вещества. Някои често срещани смеси се създават чрез разтваряне на малко количество химикал, наречен разтворено вещество в голямо количество други химикали, наречени Разтворител за да се образува решение. В този случай трябва да знаем уравнението за закона на Раул (кръстен на физика Франсоа-Мари Раул), което изглежда така: Pрешение= РРазтворителхРазтворител. В тази формула променливите представляват: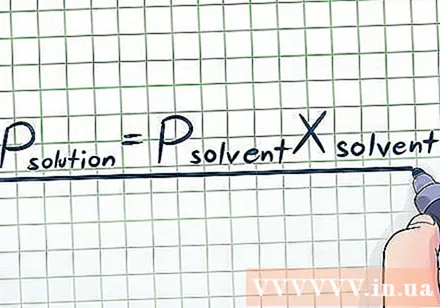
- Pрешение: Налягане на парите на целия разтвор (всички компоненти на разтвора)
- PРазтворител: Налягане на парите на разтворителя
- хРазтворител: Моларна фракция на разтворителя.
- Не се притеснявайте, ако все още не знаете термина „моларна част“ - ще го обясним в следващите стъпки.
Разграничаване на разтворители и разтворители в разтвор. Преди да изчислите парното налягане на разтвор, трябва да идентифицирате веществата, които са дадени от проблема. Обърнете внимание, че разтвор се образува, когато разтворителят се разтвори в разтворител - разтвореният химикал винаги е разтвореното вещество, а химикалът, който върши работата, е разтворителят.
- В този раздел ще вземем прост пример, за да илюстрираме горните концепции. Да предположим, че искаме да намерим парното налягане на сиропния разтвор. Обикновено сиропът се приготвя от една част захар, разтворена в една част вода, следователно казваме захарта е разтворено вещество, а водата е разтворител.
- Забележка: химическата формула на захарозата (гранулирана захар) е C12З.22О11. Ще намерите тази информация за много важна.
Намерете температурата на разтвора. Както можем да видим в гореспоменатия раздел Clausius Clapeyron, температурата на течността ще повлияе на нейното налягане на парите. Като цяло, колкото по-висока е температурата, толкова по-високо е налягането на парите - с повишаване на температурата, толкова повече течност се изпарява и увеличава налягането в съда.
- В този пример приемете, че текущата температура на сиропа е 298 К. (около 25 ° С).
Намерете налягането на парите на разтворителя. Химическите референции обикновено дават стойности на налягането на парите за много често срещани вещества и смеси, но обикновено само стойности на налягане при 25 ° C / 298 K или при температурата на кипене. Ако вашият разтвор има тази температура, тогава можете да използвате референтна стойност, в противен случай трябва да намерите налягането на парите при началната температура на разтвора.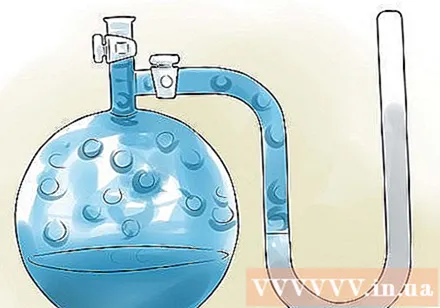
- Уравнението на Клаузий-Клапейрон може да помогне тук, използвайте налягане и температура 298 K (25 C) за P1 и T1.
- В този пример сместа има температура 25 ° C, за да можем да използваме справочна таблица. Виждаме вода при 25 ° C с налягане на парите от 23.8 mmHg
Намерете моларната фракция на разтворителя. Последното нещо, което трябва да направите, преди да решите резултатите, е да намерите моларната фракция на разтворителя. Това е доста лесно: просто преобразувайте съставките в бенки, след което намерете процента на всеки от общия брой бенки от сместа. С други думи, моларната част на всеки компонент е равна (брой молове на сместа) / (общо молове на сместа).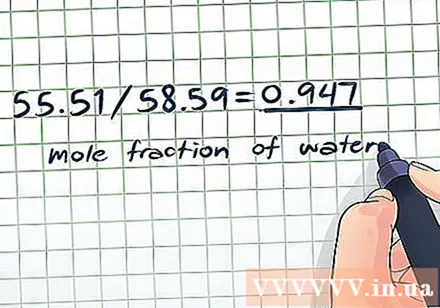
- Да приемем, че рецептата за сиропа е 1 литър (L) вода и 1 литър захароза (захар). След това трябва да намерим броя на бенките на всяка съставка. За целта ще намерим масите на всеки компонент, след което използваме моларната маса на тези компоненти, за да изработим бенки.
- Тегло (1 L вода): 1000 грама (g)
- Тегло (1 L сурова захар): Приблизително 1056,7 g
- Брой бенки (вода): 1000 грама × 1 mol / 18,015 g = 55,51 mol
- Бенки (захар): 1056,7 грама × 1 mol / 342,2965 g = 3,08 mol (Имайте предвид, че можете да намерите моларната маса на захарта от нейната химична формула, C12З.22О11.)
- Общо бенки: 55,51 + 3,08 = 58,59 мола
- Моларна фракция на водата: 55,51 / 58,59 = 0,947
Решаване на резултатите. И накрая, имаме достатъчно данни за решаване на уравнението на Раул. Това е много лесно: включете стойностите в променливи от уравнението на теоремата на Раул, споменато в началото на този раздел (Pрешение = РРазтворителхРазтворител).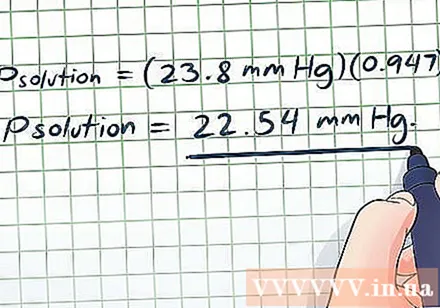
- Замествайки стойностите, имаме:
- Pрешение = (23,8 mmHg) (0,947)
- Pрешение = 22.54 mm Hg. Този резултат е разумен - в моларно изражение само малко захар се разтваря в много вода (въпреки че тези две всъщност са еднакъв обем), така че налягането на парите ще спадне само малко.
Метод 3 от 3: Намерете налягането на парата в специални случаи
Определете стандартните условия на налягане и температура. Учените често използват двойка стойности на налягането и температурата като условия по подразбиране. Тези стойности са посочени като стандартно налягане и температура (наричани общо „стандартни условия“ или DKTC). Проблемите с налягането на парата често се отнасят до DKTC, така че трябва да запомните тези стойности за удобство. DKTC се определя като:
- Температура: 273,15 K / 0 ° С / 32 F
- Налягане: 760 mmHg / 1 атм / 101 325 килопаскала
Преминете към уравнението Клаузиус-Клапейрон, за да намерите други променливи. В примера в част 1 виждаме, че уравнението на Клаузий-Клапейрон е много ефективно, когато става въпрос за изчисляване на парното налягане на чисти вещества. Не всички проблеми обаче изискват намиране на P1 или P2, но много пъти те дори искат да намерят температурата или дори стойността на ΔH.vap. В този случай, за да намерите отговора, просто трябва да превключите уравнението, така че желаната променлива да е от едната страна на уравнението, а всички останали променливи да са от другата страна.
- Да предположим например, че има неизвестна течност с налягане на парите 25 torr при 273 K и 150 torr при 325 K и ние искаме да намерим летливата енталпия на тази течност (ΔHvap). Можем да решим следното:
- ln (P1 / P2) = (ΔHvap/ R) ((1 / T2) - (1 / T1))
- (ln (P1 / P2)) / ((1 / T2) - (1 / T1)) = (ΔHvap/ R)
- R × (ln (P1 / P2)) / ((1 / T2) - (1 / T1)) = ΔHvap. Сега нека заменим стойностите:
- 8 314 J / (K × Mol) × (-1,79) / (- 0,00059) = ΔHvap
- 8 314 J / (K × Mol) × 3033,90 = ΔHvap = 25 223,83 J / mol
Вземете под внимание налягането на парите на разтвореното вещество при изпаряването му. В горния пример за закона на Раул, разтвореното ни вещество е захарта, така че тя не се изпарява сама при стайна температура (мислите ли, че някога сте виждали купа със захар да се изпарява?). Когато обаче веществото се разтвори наистина ли Ако се изпари, това ще повлияе на общото налягане на парите на разтвора. Изчисляваме това налягане, използвайки променливото уравнение на закона на Раул: Pрешение = Σ (Pсъставкахсъставка). Символът (Σ) означава, че трябва да съберем всички налягания на парите на различните компоненти, за да намерим отговор.
- Да приемем например, че имаме решение, съставено от два химикала: бензен и толуен. Общият обем на разтвора е 120 ml; 60 ml бензен и 60 ml толуен. Температурата на разтвора е 25 ° C, а налягането на парите на всеки химичен компонент при 25 ° C е 95,1 mmHg за бензен и 28,4 mmHg за толуен. За дадените стойности намерете налягането на парите на разтвора. Можем да разрешим проблема, като използваме плътността, моларната маса и налягането на парите на двата химикала:
- Обем (бензен): 60 ml = 0,06 L × 876,50 kg / 1000 L = 0,053 kg = 53 гр
- Тегло (толуен): 0,06 L × 866,90 kg / 1000 L = 0,052 kg = 52 гр
- Брой молове (бензен): 53 g × 1 mol / 78,11 g = 0,679 mol
- Брой молове (толуен): 52 g × 1 mol / 92,14 g = 0,564 mol
- Общо бенки: 0.679 + 0.564 = 1.243
- Моларна фракция (бензен): 0,679 / 1,243 = 0,546
- Моларна фракция (толуен): 0,564 / 1,243 = 0,454
- Решаване на резултатите: Pрешение = Рбензенхбензен + Pтолуенхтолуен
- Pрешение = (95,1 mmHg) (0,546) + (28,4 mmHg) (0,454)
- Pрешение = 51,92 mmHg + 12,89 mmHg = 64,81 mm Hg
Съвети
- За да използвате уравнението на Клаузиус Клапейрон по-горе, трябва да преобразувате температурата в единици на Кевин (обозначени с К). Ако имате температурата в Целзий, променете я със следната формула: тк = 273 + Т° С
- Можете да приложите горните методи, тъй като енергията съответства на количеството доставена топлина. Температурата на течността е единственият фактор на околната среда, който влияе върху налягането на парите.