Автор:
Christy White
Дата На Създаване:
8 Може 2021
Дата На Актуализиране:
1 Юли 2024

Съдържание
- Стъпвам
- Метод 1 от 3: Първа част: Разбиране на електронните обвивки
- Метод 2 от 3: Част втора: Намиране на валентни електрони в металите, с изключение на преходните метали
- Метод 3 от 3: Част трета: Намиране на валентни електрони в преходни метали
- Съвети
- Необходимост
Валентните електрони лежат във външната обвивка на елемент. Броят на валентните електрони в атома определя вида на химическата връзка, която този елемент може да образува. Най-добрият начин да разберете броя на валентните електрони е да използвате периодичната таблица на елементите.
Стъпвам
Метод 1 от 3: Първа част: Разбиране на електронните обвивки
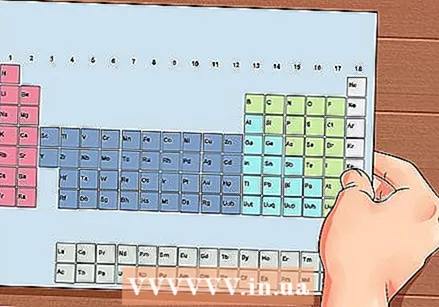 Периодичната система на елементите. Това е таблица с цветни кодове, където във всяка клетка се показва елемент с атомния номер и 1 до 3 букви като символ.
Периодичната система на елементите. Това е таблица с цветни кодове, където във всяка клетка се показва елемент с атомния номер и 1 до 3 букви като символ. 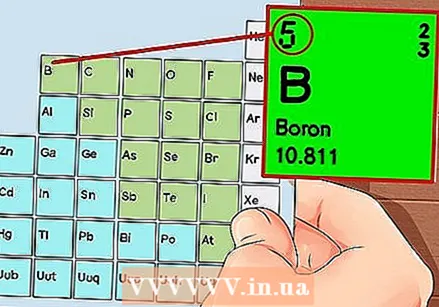 Намерете атомния номер на елемента. Атомният номер е над или до символа на елемента. Например: Бор (В) има атомен номер 5, което означава, че има 5 протона и 5 електрона.
Намерете атомния номер на елемента. Атомният номер е над или до символа на елемента. Например: Бор (В) има атомен номер 5, което означава, че има 5 протона и 5 електрона. 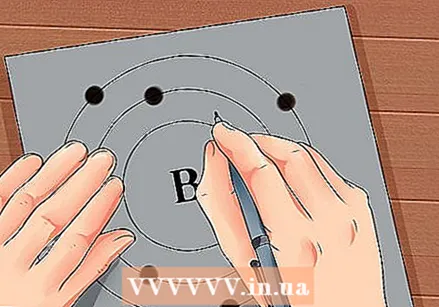 Начертайте просто представяне на атом и поставете електроните в орбита около ядрото. Тези работни места се наричат още черупки или енергийни нива. Максималният брой електрони, които могат да бъдат в една и съща обвивка, е фиксиран и черупките се запълват от вътрешната към външната орбита.
Начертайте просто представяне на атом и поставете електроните в орбита около ядрото. Тези работни места се наричат още черупки или енергийни нива. Максималният брой електрони, които могат да бъдат в една и съща обвивка, е фиксиран и черупките се запълват от вътрешната към външната орбита. - K Черупка (вътрешна): максимум 2 електрона.
- L черупка: максимум 8 електрона.
- M черупка: максимум 18 електрона.
- N обвивка: максимум 32 електрона.
- O Черупка: максимум 50 електрона.
- P Shell (външен): максимум 72 електрона.
 Намерете броя на електроните във външната обвивка. Това са валентните електрони.
Намерете броя на електроните във външната обвивка. Това са валентните електрони. - Когато валентната обвивка е пълна, елементът е стабилен.
- Ако валентната обвивка не е пълна, тогава елементът реагира, което означава, че може химически да се свърже с атома на друг елемент. Всеки атом споделя своите валентни електрони в опит да напълни валентната обвивка.
Метод 2 от 3: Част втора: Намиране на валентни електрони в металите, с изключение на преходните метали
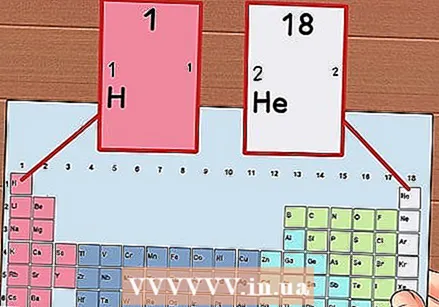 Номерирайте всяка колона на периодичната таблица от 1 до 18. Водородът (H) е в горната част на колона 1, а хелийът (He) в горната част на колона 18. Това са различните групи елементи.
Номерирайте всяка колона на периодичната таблица от 1 до 18. Водородът (H) е в горната част на колона 1, а хелийът (He) в горната част на колона 18. Това са различните групи елементи. 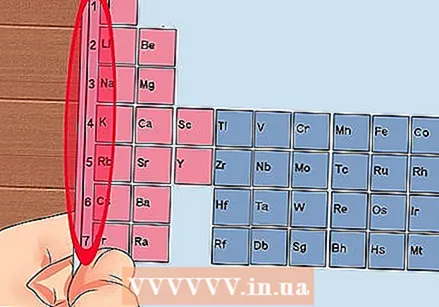 Дайте на всеки ред число от 1 до 7. Това са периодите на елементите и те съответстват на броя на черупките или енергийните нива на атома.
Дайте на всеки ред число от 1 до 7. Това са периодите на елементите и те съответстват на броя на черупките или енергийните нива на атома. - Водородът (H) и хелийът (He) имат и една обвивка, докато Francium (Fr) има 7.
- Лантанидите и актиноидите са групирани и изброени под основната таблица. Всички лантаниди принадлежат към Период 6, Група 3 и всички актиноиди принадлежат към Период 7, Група 3.
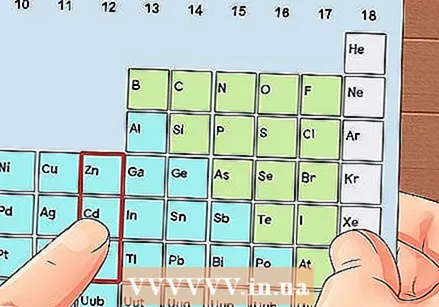 Намерете елемент, който не е преходен метал. Преходните метали са в групи от 3 до 12. Груповите номера на другите метали показват броя на валентните електрони.
Намерете елемент, който не е преходен метал. Преходните метали са в групи от 3 до 12. Груповите номера на другите метали показват броя на валентните електрони. - Група 1: 1 валентен електрон
- Група 2: 2 валентни електрона
- Група 13: 3 валентни електрона
- Група 14: 4 валентни електрона
- Група 15: 5 валентни електрона
- Група 16: 6 валентни електрона
- Група 17: 7 валентни електрона
- Група 18: 8 валентни електрона - с изключение на хелий, който има 2
Метод 3 от 3: Част трета: Намиране на валентни електрони в преходни метали
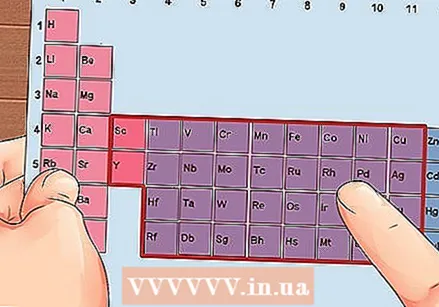 Намерете елемент от групи 3 до 12, преходните метали.
Намерете елемент от групи 3 до 12, преходните метали. Определете броя на валентните електрони въз основа на номера на групата. Тези групови числа съответстват на възможен брой валентни електрони.
Определете броя на валентните електрони въз основа на номера на групата. Тези групови числа съответстват на възможен брой валентни електрони. - Група 3: 3 валентни електрона
- Група 4: 2 до 4 валентни електрона
- Група 5: 2 до 5 валентни електрона
- Група 6: 2 до 6 валентни електрона
- Група 7: 2 до 7 валентни електрона
- Група 8: 2 или 3 валентни електрона
- Група 9: 2 или 3 валентни електрона
- Група 10: 2 или 3 валентни електрона
- Група 11: 1 или 2 валентни електрона
- Група 12: 2 валентни електрона
Съвети
- Преходните метали могат да имат валентни черупки, които не са напълно пълни. Определянето на точния брой на валентните електрони в преходните метали изисква определени принципи на квантовата теория, които са извън обхвата на тази статия.
Необходимост
- Периодична таблица на елементите
- Молив
- Хартия