Автор:
Virginia Floyd
Дата На Създаване:
6 Август 2021
Дата На Актуализиране:
1 Юли 2024

Съдържание
- Стъпки
- Метод 1 от 3: Основите
- Метод 2 от 3: Определяне на типа връзка чрез електроотрицателност
- Метод 3 от 3: Изчисляване на Mulliken електроотрицателност
- Съвети
В химията електроотрицателността е способността на атомите да привличат електрони от други атоми към тях. Атом с висока електроотрицателност силно привлича електрони, а атом с ниска електроотрицателност привлича електрони слабо. Стойностите на електроотрицателност се използват за прогнозиране на поведението на различни атоми в химичните съединения.
Стъпки
Метод 1 от 3: Основите
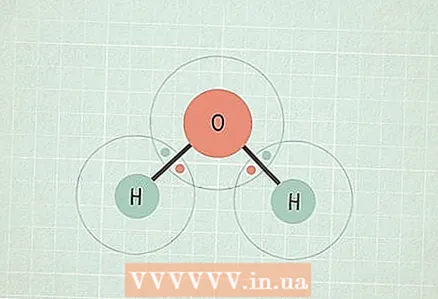 1 Химически връзки. Такива връзки възникват, когато електроните в атомите взаимодействат помежду си, тоест два електрона (по един от всеки атом) стават общи.
1 Химически връзки. Такива връзки възникват, когато електроните в атомите взаимодействат помежду си, тоест два електрона (по един от всеки атом) стават общи. - Описание на причините за взаимодействието на електрони в атомите е извън обхвата на тази статия.За повече информация по тази тема прочетете например тази статия.
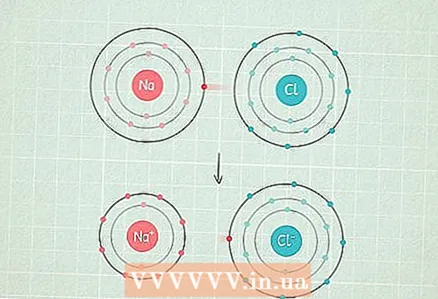 2 Ефект на електроотрицателност. Когато два атома привличат електроните един към друг, силата на привличане не е еднаква. Атом с по -висока електроотрицателност привлича два електрона по -силно. Атом с много висока електроотрицателност привлича електрони с такава сила, че вече не говорим за споделени електрони.
2 Ефект на електроотрицателност. Когато два атома привличат електроните един към друг, силата на привличане не е еднаква. Атом с по -висока електроотрицателност привлича два електрона по -силно. Атом с много висока електроотрицателност привлича електрони с такава сила, че вече не говорим за споделени електрони. - Например, в молекулата на NaCl (натриев хлорид, обикновена сол), хлорният атом има доста висока електроотрицателност, а натриевият атом е доста нисък. Така че електроните са привлечени от хлорния атом и отблъскват натриевите атоми.
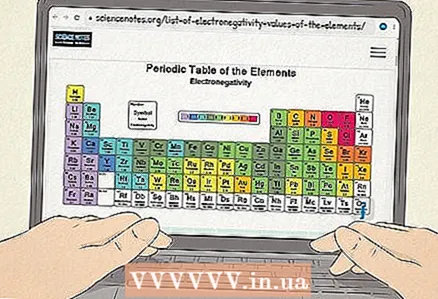 3 Таблица за електроотрицателност. Тази таблица включва химически елементи, подредени по същия начин, както в периодичната таблица, но за всеки елемент е дадена електроотрицателността на неговите атоми. Такава таблица може да бъде намерена в учебници по химия, справочни материали и в мрежата.
3 Таблица за електроотрицателност. Тази таблица включва химически елементи, подредени по същия начин, както в периодичната таблица, но за всеки елемент е дадена електроотрицателността на неговите атоми. Такава таблица може да бъде намерена в учебници по химия, справочни материали и в мрежата. - Тук ще намерите отлична таблица за електроотрицателност. Обърнете внимание, че той използва скалата за електроотрицателност на Полинг, която е най -често срещаната. Съществуват обаче и други начини за изчисляване на електроотрицателността, един от които ще бъде разгледан по -долу.
 4 Тенденции на електроотрицателност. Ако нямате под ръка таблица за електроотрицателност, можете да оцените електроотрицателността на атом по местоположението на елемент в периодичната таблица.
4 Тенденции на електроотрицателност. Ако нямате под ръка таблица за електроотрицателност, можете да оцените електроотрицателността на атом по местоположението на елемент в периодичната таблица. - Как надясно елементът се намира, Повече ▼ електроотрицателността на неговия атом.
- Как по-висок елементът се намира, Повече ▼ електроотрицателността на неговия атом.
- По този начин атомите на елементите, разположени в горния десен ъгъл на периодичната таблица, имат най -високите електроотрицателности, а атомите на елементите, разположени в долния ляв ъгъл, имат най -ниските.
- В нашия пример за NaCl можем да кажем, че хлорът има по -висока електроотрицателност от натрия, тъй като хлорът се намира вдясно от натрия.
Метод 2 от 3: Определяне на типа връзка чрез електроотрицателност
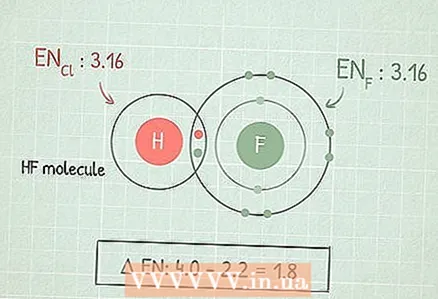 1 Изчислете разликата между електроотрицателностите на два атома, за да разберете характеристиките на връзката между тях. За да направите това, извадете по -малката електроотрицателност от по -голямата.
1 Изчислете разликата между електроотрицателностите на два атома, за да разберете характеристиките на връзката между тях. За да направите това, извадете по -малката електроотрицателност от по -голямата. - Например, помислете за молекулата на HF. Извадете електроотрицателността на водорода (2.1) от електроотрицателността на флуора (4.0): 4.0 - 2.1 = 1,9.
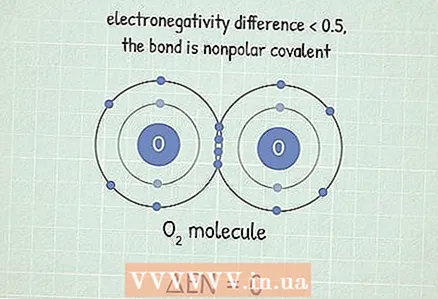 2 Ако разликата е по-малка от 0,5, тогава връзката е ковалентна неполярна, при която електроните се привличат с почти същата сила. Такива връзки се образуват между два еднакви атома. Неполярните връзки обикновено са много трудни за прекъсване. Това е така, защото атомите споделят електрони, което прави връзката им стабилна. Необходима е много енергия, за да се унищожи.
2 Ако разликата е по-малка от 0,5, тогава връзката е ковалентна неполярна, при която електроните се привличат с почти същата сила. Такива връзки се образуват между два еднакви атома. Неполярните връзки обикновено са много трудни за прекъсване. Това е така, защото атомите споделят електрони, което прави връзката им стабилна. Необходима е много енергия, за да се унищожи. - Например молекулата О2 има този тип връзка. Тъй като два кислородни атома имат еднаква електроотрицателност, разликата между тях е 0.
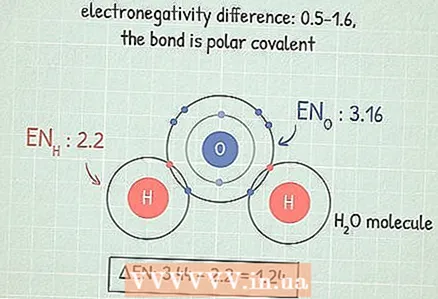 3 Ако разликата е в диапазона 0,5 - 1,6, тогава връзката е ковалентна полярна. В този случай един от двата атома привлича електрони по -силно и следователно придобива частичен отрицателен заряд, а другият частичен положителен заряд. Този дисбаланс на заряда позволява на молекулата да участва в определени реакции.
3 Ако разликата е в диапазона 0,5 - 1,6, тогава връзката е ковалентна полярна. В този случай един от двата атома привлича електрони по -силно и следователно придобива частичен отрицателен заряд, а другият частичен положителен заряд. Този дисбаланс на заряда позволява на молекулата да участва в определени реакции. - Например молекулата Н2O (вода) има този тип връзка. Атомът О е по -електроотрицателен от два Н атома, така че кислородът привлича електрони по -силно и придобива частичен отрицателен заряд, а водородът - частичен положителен заряд.
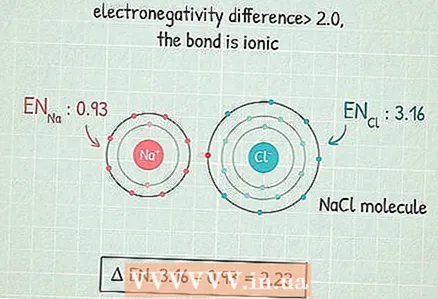 4 Ако разликата е по -голяма от 2,0, тогава връзката е йонна. Това е връзка, при която общата електронна двойка преминава предимно към атом с по -висока електроотрицателност, който придобива отрицателен заряд, а атом с по -ниска електроотрицателност придобива положителен заряд. Молекулите с такива връзки реагират добре с други атоми и дори могат да бъдат унищожени от полярни атоми.
4 Ако разликата е по -голяма от 2,0, тогава връзката е йонна. Това е връзка, при която общата електронна двойка преминава предимно към атом с по -висока електроотрицателност, който придобива отрицателен заряд, а атом с по -ниска електроотрицателност придобива положителен заряд. Молекулите с такива връзки реагират добре с други атоми и дори могат да бъдат унищожени от полярни атоми. - Например, молекулата NaCl (натриев хлорид) има този тип връзка.Хлорният атом е толкова електроотрицателен, че привлича двата електрона към себе си и придобива отрицателен заряд, а натриевият атом придобива положителен заряд.
- NaCl може да бъде унищожен от полярна молекула като H2O (вода). Във водна молекула водородната страна на молекулата е положителна, а кислородната страна е отрицателна. Ако смесите солта с водата, водните молекули разграждат молекулите на солта, което я кара да се разтваря.
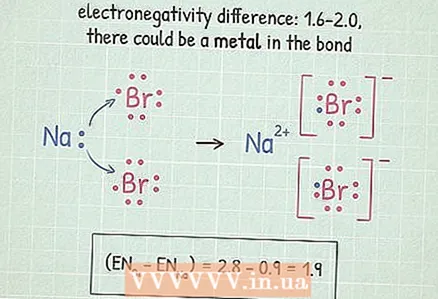 5 Ако разликата е между 1,6 и 2,0, проверете за метал. Ако метален атом присъства в молекула, тогава връзката е йонна. Ако в молекулата няма метални атоми, тогава връзката е полярна ковалентна.
5 Ако разликата е между 1,6 и 2,0, проверете за метал. Ако метален атом присъства в молекула, тогава връзката е йонна. Ако в молекулата няма метални атоми, тогава връзката е полярна ковалентна. - Металите се намират вляво и в центъра на периодичната таблица. В тази таблица металите са подчертани.
- В нашия пример за ВЧ разликата между електроотрицателностите попада в този диапазон. Тъй като H и F не са метали, връзката полярна ковалентна.
Метод 3 от 3: Изчисляване на Mulliken електроотрицателност
 1 Намерете първата йонизационна енергия на атом. Скалата за електроотрицателност на Мъликен е малко по -различна от скалата на Полинг, спомената по -горе. Първата йонизационна енергия е необходима за отстраняване на един атом от електрон.
1 Намерете първата йонизационна енергия на атом. Скалата за електроотрицателност на Мъликен е малко по -различна от скалата на Полинг, спомената по -горе. Първата йонизационна енергия е необходима за отстраняване на един атом от електрон. - Значението на такава енергия може да се намери в справочниците по химия или в мрежата, например тук.
- Като пример, нека открием електроотрицателността на литий (Li). Първата й йонизационна енергия е 520 kJ / mol.
 2 Намерете енергията на афинитет към електрон. Това е енергията, освободена в процеса на свързване на електрон към атом. Значението на такава енергия може да се намери в справочниците по химия или в мрежата, например тук.
2 Намерете енергията на афинитет към електрон. Това е енергията, освободена в процеса на свързване на електрон към атом. Значението на такава енергия може да се намери в справочниците по химия или в мрежата, например тук. - Енергията на афинитета на електроните на лития е 60 kJ / mol.
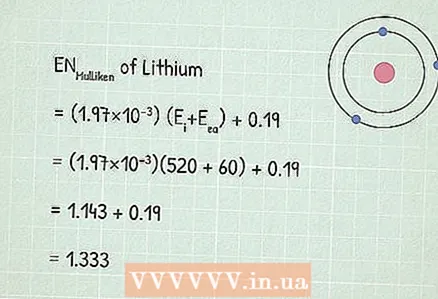 3 Използвайте уравнението за електроотрицателност на Мъликен:RUМуликен = (1,97 × 10) (напрi+ Дда) + 0,19.
3 Използвайте уравнението за електроотрицателност на Мъликен:RUМуликен = (1,97 × 10) (напрi+ Дда) + 0,19. - В нашия пример:
- RUМуликен = (1,97 × 10) (напрi+ Дда) + 0,19
- RUМуликен = (1,97×10)(520 + 60) + 0,19
- RUМуликен = 1,143 + 0,19 = 1,333
- В нашия пример:
Съвети
- В допълнение към скалите на Полинг и Мюликен, има скали на електроотрицателност според Allred-Rochow, Sanderson, Allen. Всички те имат свои собствени формули за изчисляване на електроотрицателност (някои от тях са доста сложни).
- Електроотрицателността няма мерни единици.